Дата добавления: 2009-07-07
Автор статьи: Michael R. Lucey, M.D., Philippe Mathurin, M.D., Ph.D., and Timothy R. Morgan, M.D.
Алкогольный гепатит.
Чрезмерное потребление алкоголя является третьей лидирующей причиной смерти в США. Алкоголь ассоциированная смертность непропорционально высока среди молодого населения и примерно 30 лет жизни теряется в результате алкоголь ассоциированной смерти, или суммарно, 2,3 миллиона лет потенциальной жизни потеряно в 2001 году в США. Чрезмерное потребление алкоголя приводит к краткосрочным и долгосрочным поражениям печени, нескольким видам рака, непреднамеренным травмам на рабочем месте и на дороге, домашнему и социальному насилию, распаду браков и нарушению социальных и семейных взаимоотношений.
Связь между приемом алкоголя и алкогольной болезнью печени, к настоящему времени, хорошо документирована, хотя цирроз печени развивается лишь у немногих сильно пьющих людей. Риск развития цирроза пропорционально повышается при употреблении более чем 30 г алкоголя в день, самый высокий риск связан с употреблением более 120 г в день. Распространенность цирроза 1% при употреблении от 30 до 60 г в сутки увеличивается до 5,7% при употреблении 120 г в сутки. Следует заметить, что такие факторы, как пол, генетические характеристики, воздействие окружающей среды (включая хронические вирусные инфекции), играют роль в генезе алкогольной болезни печени.
Хроническое употребление алкоголя вызывает несколько типов поражения печени. Регулярное употребление, даже в течение нескольких дней, может привести к ожирению печени (известному так же как стеатоз), расстройство при котором гепатоциты содержат макровезикулярные капли триглицеридов. Хотя алкогольная жировая дистрофия уменьшается при воздержании, стеатоз предрасполагает человека продолжающего употреблять алкоголь к фиброзу и циррозу печени. Этот обзор посвящен алкогольному гепатиту, курабельной форме алкогольной болезни печени. В виду того, что до 40% пациентов с тяжелыми алкогольными гепатитами умирают в течение 6 месяцев после начала развития клинического синдрома, необходимы соответствующий диагноз и лечение.
Клинические проявления алкогольного гепатита.
Алкогольный гепатит - это клинический синдром, сопровождающийся желтухой и печеночной недостаточностью, которые имеют место после десятков дней массивного употребления алкоголя (более 100г в сутки). Не редко пациент может закончить прием алкоголя за несколько недель до начала развития симптомов. Типичный возраст для подобных проявлений 40 – 60 лет. Хотя женский пол является независимым фактором в развитии алкогольного гепатита, больше мужчин предпочитают большие дозы и больше мужчин, чем женщин страдают алкогольной болезнью печени. Тип принимаемого алкоголя не влияет на риск развития алкогольного гепатита. Заболеваемость не известна, но среди 1604 пациентов с алкоголизмом, которым производилась биопсия печени, распространенность достигла 20%.
Кардинальный признак алкогольного гепатита – быстрое развитие желтухи. Другие характерные признаки и симптомы - лихорадка, асцит, дистрофия проксимальных мышц. У пациентов с тяжелым алкогольным гепатитом может развиваться энцефалопатия. Типична увеличенная и дряблая печень.
Лабораторные показатели аспартат аминотрансферазы более чем в 2 раза выше нормы, хотя редко более 300 IU в миллилитре, в то время как сывороточная аланин аминотрансфераза ниже. Отношение АсТ/АлТ обычно более 2-х, хотя это явление скорее специфично, чем характерно. Предположительный механизм возникновения такой большой разницы в снижении печеночной аланин аминотрансферазной активности, алкоголь индуцированном истощении пиридоксал-5’-фосфата и повышении печеночного митохондриального аспартата. Число белых кровяных клеток в периферической крови, число нейтрофилов, уровень общего сывороточного билирубина, и международное нормализованное отношение (INR, отношение времени свертывания у пациента к нормальному времени свертывания) повышены. Зловещим признаком является повышение уровня сывороточного креатинина, так как это часто предвестник развития гепаторенального синдрома и смерти.
Микроскопически, у пациентов с алкогольным гепатитом отмечается гепатоцеллюлярное повреждение характеризующееся вздутием (опуханием) гепатоцитов, которые часто содержат эозинофильные тельца, называемые тельцами Мэллори (Mallory) (так же известные как алкогольный гиалин), окруженных нейтрофилами (Рисунок 1). Присутствие больших жировых глобул в гепатоцитах так же известное как стеатоз показательно для алкогольного гепатита. Характерным поражением при алкогольном гепатите является интрасинусоидальный фиброз (то есть, очевидно, фиброз в пространстве между эндотелиальными клетками и гепатоцитами). Перивенулярный фиброз, перипортальный фиброз и цирроз, которые типичны для алкогольного фиброза, часто сопутствуют алкогольному гепатиту. Дополнительные гистологические признаки, ассоциированные с алкогольным гепатитом, включают пенистую дегенерацию гепатоцитов и острый склерозирующий гиалиновый некроз.
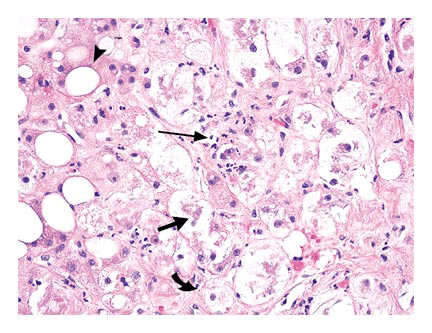
Рисунок 1. Гистопатологические признаки печеночного биоптата пациента с алкогольным гепатитом.
Алкогольный гепатит характеризуется гепатоцеллюлярным повреждением с вздутием гепатоцитов (изогнутая стрелка). Некоторые гепатоциты содержат жировые капли (стеатоз, указатель стрелки), тогда как другие могут содержать внутриклеточные, аморфные, эозинофильные тельца Мэллори (короткая стрелка), они часто окружены нейтрофилами (длинная стрелка) (гематоксилин и эозин).
Неалкогольный стеатогепатит сопровождает ожирение и инсулинорезистентность, при этом у него много общего с алкогольным гепатитом, включая вздутие гепатоцитов, стеатоз, тельца Меллори, воспаление, интрасинусоидальный коллаген и фиброз, или цирроз. Однако тяжесть этих изменений обычно больше при алкогольном гепатите, и холестаз – частое проявление алкогольного гепатита не имеет места при неалкогольном стеатогепатите. Микроскопия биоптата печени обычно не позволяет установить первичную причину стеатоза, телец Меллори и фиброза у пациентов с ожирением и чрезмерной алкоголизацией.
Восстановление при алкогольном гепатите обусловлено в основном воздержанием от алкоголя, наличием легкого клинического синдрома, и осуществлением надлежащего лечения. В течение нескольких недель после прекращения приема алкоголя желтуха и лихорадка могут уменьшиться, но асцит и печеночная энцефалопатия могут персистировать месяцы и годы. Как не купирующаяся желтуха, так и развитие почечной недостаточности свидетельствуют о плохом прогнозе. К сожалению, даже если пациент придерживается всех предписаний, излечение алкогольного гепатита не гарантировано.
Диагностика алкогольного гепатита.
Сочетание повышенного уровня АсТ (но не более 300 IU в мл.) и отношения АсТ/АлТ большего 2-х, при уровне общего сывороточного билирубина более 5 мг/длитр (86мМ/л) и повышении INR, нейтрофилии у пациента с асцитом и тяжелым алкогольным анамнезом показательно для алкогольного гепатита пока не доказано обратное. В некоторых случаях может потребоваться опрос родственников или знакомых для подтверждения алкоголизации.
Дифдиагностику алкогольного гепатита проводят с неалкогольным стеатозом, острым или хроническим вирусным гепатитом, медикаментозным поражением печени, фульминантным течением болезни Вильсона, аутоиммунным поражением печени, дефицитом alpha-1 антитрипсина, гнойным абсцессом печени, восходящим холангитом, декомпенсацией гепатоцеллюлярной карциномы.
Вышеописанные признаки алкогольного гепатита в биоптате печени могут помочь исключить другие причины заболевания печени, но биопсия не обязательная процедура для постановки диагноза. Риск кровотечения во время и после биопсии может быть снижен за счет трансюгулярного доступа. Биопсия печени не рекомендуется для подтверждения, или опровержения абстиненции, так как определить временной период по гистологическим признакам достаточно трудно.
Пациенты должны быть обследованы на предмет бактериальных инфекций, таких как пневмония, спонтанный бактериальный перитонит, инфекции мочевого тракта путем исследования культур крови, мочи, асцитической жидкости при её наличии. Рентгенограмма органов грудной клетки так же необходима. УЗИ печени полезно для исключения абсцесса, скрытой гепатоцеллюлярной карциномы и билиарной обструкции, все эти состояния могут скрываться под маской алкогольного гепатита. Так же УЗИ можно комбинировать с аспирацией асцитической жидкости. Доплеровское исследование потока может оказаться полезным, поскольку повышение пиковой систолической скорости, или увеличение диаметра печеночной артерии подтверждает диагноз.
Определение тяжести алкогольного гепатита.
Для определения тяжести алкогольного гепатита и проведения лечения использовались различные оценочные системы (Таблица 1). Дискриминантная функция Мадрея, шкала Глазго и шкала, основанная на Модели Терминальной фазы Болезни Печени (Model for End-Stage Liver Disease - MELD) помогают клинически определить следует ли начинать кортикостероиды, тогда как шкала Лилл (или модель) разработана, чтобы определить стоит ли прекратить назначать кортикостероиды после недельного курса. Эти оценочные системы имеют общие элементы, такие как уровень сывороточного билирубина и протромбиновое время (или INR) (Таблица 1). Дискриминантная функция Маддрея имеет преимущество использоваться длительно, но её, может быть, трудно оценивать, если доступно только INR, без протромбинового времени (фактического и контрольного). Шкала Глазго, по крайней мере, в одном исследовании показала, какие пациенты с высоким значением дискриминантной функции Мадрея получат пользу от кортикостероидов. Шкала MELD проста для определения (см. www.mayoclinic.org/meld/mayomodel7.html; выше показатель MELD хуже прогноз), и её полезность была подтверждена в ретроспективных исследованиях. Полезность шкалы Глазго и Лила должна быть проверена на популяциях других стран.
Таблица 1. Компоненты оценочных систем для оценки тяжести алкогольного гепатита.
Дискриминантная функция Мадрея вычисляется по формуле [4,6*(протромбиновое время пациента – контрольное протромбиновое время, в секундах)] + уровень сывороточного билирубина, в мг/длитр. Значение большее 32 свидетельствует о тяжелом алкогольном гепатите и является пороговым для назначения кортикостероидов. В 2005 исследователи из Глазго сообщили о последовательном логистически-регрессивном анализе идентифицирующем вариабельность относительного 28 и 84 дневного выживания после выписки на большом числе пациентов с алкогольным гепатитом; на основе результатов, они разработали новый оценочный инструмент, названный Глазговская шкала алкогольного гепатита (чтобы не путать со шкалой ком Глазго). В этом инструменте для выявления пациентов с наибольшим риском смертельного исхода в отсутствие лечения, для отбора нуждающихся в кортикостероидах, оцениваются возраст, содержание белых клеток в периферической крови, концентрация азота и билирубина в моче, протромбиновое время или INR. В результате исследования было показано, что 84 дневная выживаемость пациентов, получивших более 32 по дискриминантной функции Мадрея и более 9 по Глазговской шкале алкогольного гепатита, составила 59% в сравнение с 38% среди не получавших лечение.
Некоторые пациенты с алкогольным гепатитом становятся кандидатами на пересадку печени. Шкала MELD основанная на цифровой шкале предсказывает риск смерти пациента во время ожидания трансплантата, шкала основана на сывороточном уровне креатинина билирубина и INR. В двух ретроспективных исследованиях шкала MELD предсказывала краткосрочную смертность среди пациентов с алкогольным гепатитом так же, или лучше дискриминантной функции Мадрея. 21 бал по MELD сопровождался 90 дневной смертностью 20% пациентов, Данн и др. предложили уровень в 21 бал использовать для проведения испытаний «потенциальных терапевтических агентов».
Шкала Лилла, основанная на данных до лечения и ответе сывороточного уровня билирубина на недельный курс кортикостероидов, может использоваться для прекращения назначения кортикостероидов из-за недостаточного эффекта.
Механизмы связанного с алкоголем поражения печени.
Алкоголь метаболизируется в гепатоцитах путем окисления в ацетальдегид и, впоследствии, из ацетальдегида в ацетат. Окислительный метаболизм алкоголя создает избыток восстановительных эквивалентов, в первую очередь в форме восстановленного никотинамида аденина динуклеотида (НАД) – НАДH. Изменение окисления-восстановления НАДH – НАД+ способно в печени ингибировать окисление жирных кислот и цикл трикарбоновых кислот и может способствовать липогенезу. В дополнение этанол способствует метаболизму липидов путем торможения пероксисомальной пролиферации активированного alpha-рецептора (ППАР) и АМФ киназы и стимуляции регулируемого стеролом элемент -связывающего фактора-1, мембрана - связанного фактора транскрипции. В комбинации эти эффекты приводят к жиро накопительному метаболическому ремоделированию печени. Не смотря на то, остаётся загадкой, как сам алкоголь связан с развитием алкогольной болезни печени.
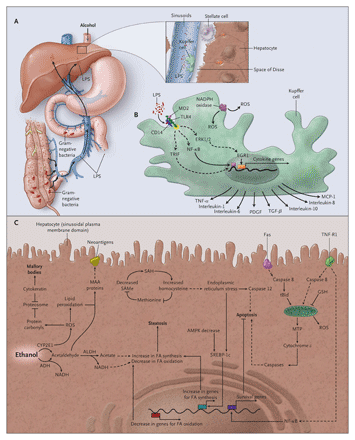
Рисунок 2. Аспекты патофизиологии алкоголь – индуцированного поражения печени.
Этанол способствует перемещению липополисахаридов (LPS) из просвета тонкого и толстого кишечника в портальную вену, откуда они попадают в печень (Panel A). Нормальная печень состоит из синусоид выстеленных эндотелиальными клетками. Купферовы клетки расположены в синусоидах, тогда как звездчатые клетки находятся между эндотелиоцитами и гепатоцитами (Panel B). В клетках Купфера липополисахара связываются с CD14, которые соединяются с толл-подобными рецепторами 4 (TLR4), в конечном итоге активирующие множественные цитокиновые гены. NADPH оксидаза вырабатывает реактивные кислородные частицы (ROS), которые активируют цитокиновые гены внутри Купферовских клеток и могут воздействовать на гепатоциты и звездчатые клетки печени. Такие цитокины, как фактор некроза опухоли -alpha (TNF-alpha) имеют как паракринные эффекты на гепатоциты, так и системные такие, как лихорадка, анорексия, потеря массы тела. Интерлейкин -8 и моноцитарный хемотаксический протеин-1 (MCP-1) притягивает нейтрофилы и макрофаги. Тромбоцитарный фактор роста (PDGF) и трансформирующий фактор роста бета (TGF-b) способствуют активации, миграции и делению звездчатых клеток печени, увеличивая печеночный фиброз. В гепатоцитах этанол превращается в ацетальдегид под действием цитозольного фермента алкоголь дегидрогеназы (ADH) и микросомального фермента цитохрома P-450 2E1 (CYP2E1) (Panel C). Ацетальдегид превращается в ацетат. Эти реакции производят NADH и тормозят окисление триглицеридов и жирных кислот. ROS выработанные CYP2E1 и митохондриях вызывают перекисное окисление липидов и образование белковых карбонилов. Продукты перекисного окисления липидов могут соединяться с ацетальдегидом и протеинами с образованием неоантигенов, которые способны стимулировать аутоиммунный ответ. Торможение протеосом уменьшает катаболизм поврежденных белков, и могут способствовать накоплению цитокератина и образованию телец Мэллори. Уменьшение ферментов превращающих гомоцистеин в метионин повышает концентрацию гомоцистеина, подвергая стрессу эндоплазматический ретикулум. Транскрипционный фактор (SREBP-1c) высвобождается из эндоплазматического ретикулума вследствие его стресса и инициирует транскрипцию генов ответственных за синтез триглицеридов и жирных кислот. Уменьшение связывания пероксисомальной пролиферации активированного alpha-рецептора (PPAR-alpha) с ДНК снижает экспрессию генов вовлеченных в окисление жирных кислот. Транспорт глутатиона из цитозоля в митохондрии снижен. Активация Fas и TNF рецептора 1 (TNF-R1) стимулирует каспазу 8, вызывая повреждение митохондрий и открытию митохондриальных транспортных пор (MTP), высвобождение цитохрома C и активацию каспаз, которые способствуют апоптозу. Активация TNF-R1 ведет к активации нуклеарного фактора kB (NF-kB) и экспрессии генов поддерживающих выживание клеток. В Panels B и C сплошными линиями показаны установленные пути и пунктирными линиями показаны косвенные и предполагаемые взаимоотношения между объектами. ALDH означает aldehyd dehydrogenase, AMPK AMP -активированная протеин киназа, EGR1 – гены раннего ответа 1, ERK -экстрацеллюлярные сигнал-регулируемые киназы, FA – жирные кислоты, GSH - глютатион, MAA малондиалдегид-ацетальдегид аддукт, SAH S-adenosylhomocystein, SAMe S-adenosyl-L-methionin, and TRIF толл-интерлейкин - 1R - доменсодержащего адаптер - индуцированного интерферона бета.
Недавние продвижения в нашем понимании патогенеза алкоголь индуцированного поражения печени и развитие новых подходов к его лечению получены при изучении животных, использовании множества непосредственных инфузий алкоголя и жиров в желудок крыс и мышей, которые приводят к поражению печени, напоминающему легкий алкогольный гепатит у человека, тем не менее, с небольшим фиброзом. Эндотоксин, биологическая активность которого связана с липополисахаридами (LPS), компонент наружной стенки грамотрицательных бактерий – ключевой момент воспалительного процесса в этой экспериментальной модели. Проницаемость кишечника, состоящая из нескольких факторов, таких как усиление, или ограничение перемещения, или транспорта LPS-эндотоксина из просвета кишечника в кровь портальной вены, оказалось, изменяется при длительной экспозиции алкоголя. Предварительное лечение антибиотиками с целью очищения кишечника от флоры, или лактобактериями для репопуляции кишечника может аннулировать рост LPS-эндотоксина, который имеет место при инфузии алкоголя и жиров, и может свести на нет поражение печени. Так же у человека проницаемость кишечника и уровень циркулирующего LPS-эндотоксина повышается у пациентов с алкогольным поражением печени.
Когда LPS-эндотоксин попадает в кровь портальной вены, он связывается с LPS-связывающим белком, это обязательное условие для воспаления и гистопатологического ответа на воздействие алкоголя в экспериментальной модели. LPS-LPS-связанный протеиновый комплекс связывается с рецептором CD14 клеточной мембраны Купферовских клеток печени (Figure 2B). Купферовские клетки – основа развития алкогольного гепатита в экспериментальной модели. Активация Купферовских клеток LPS-эндотоксином требует наличия трех клеточных протеинов: CD14 (так же известный, как антиген дифференцировки моноцитов), toll-подобный рецептор 4 (TLR4), и протеин MD2, который ассоциируется с TLR4 для связывания с LPS–LPS-связанным протеином. Предшественники TLR4 включают активацию раннего ответа 1 (EGR1), непосредственный ранний gene–zinc-finger фактор транскрипции, ядерный фактор kB (NF-kB), и TLR4 адаптер, известный как TRIF толл-интерлейкин - 1R - доменсодержащего адаптер - индуцированного интерферона бета. EGR1 играет ключевую роль в липополисахарид-стимулированной TNF-alpha продукции; у мышей отсутствие этого предотвращает алкогольное поражение печени. TRIF-зависимая сигнальная молекула (но не миелоид дифференцирующий фактор 88 [MyD88]) способствует алкоголь индуцированному повреждению печени стимулируемому TLR4. MyD88 – это адапторный протеин, участвующий во многих толл-подобных рецепторных сигнальных путях.
Потребление алкоголя повышает экскрецию маркеров окислительного стресса, и у человека, самый высокий уровень отмечается в случае алкогольного гепатита. Исследования на мышах и крысах говорят о том, что активированные Купферовские клетки и гепатоциты являются источником свободных радикалов (особенно реактивных кислородных промежуточных форм), которые вырабатываются в ответ на короткие и продолжительные экспозиции алкоголя. Окислительный стресс стимулирует алкогольное повреждение печени, по крайней мере, через изменение активности цитохрома P-450 2E1, повреждение митохондрий, активацию эндоплазматический ретикулум активированного апоптоза и усиление синтеза липидов.
TNF-alpha, выработанный в Купферовских клетках, оказалось играет ключевую роль в развитии алкогольного гепатита. Уровень циркулирующего TNF-alpha выше у пациентов с алкогольным гепатитом, чем у тяжело пьющих с неактивным циррозом, тяжело пьющих без болезни печени, и людей без алкоголизма и заболевания печени, и имеет высокую корреляцию со смертностью. В одном исследовании повышалась экспрессия гена TNF-alpha в ткани печени пациентов с тяжелым алкогольным гепатитом. Повреждение печени в значительной степени уменьшалось, когда алкоголь и жир давали TNF рецептор 1 (TNF-R1) – блокированным крысам и мышам, которых лечили anti-TNF-alpha антителами или талидомидом (который уменьшает продукцию TNF-alpha).
TNF-alpha индуцированная цитотоксичность стимулируется через TNF-R1 (Figure 2C). Пероксидазная емкость TNF-alpha в гепатоцитах ограничивается в митохондриях и увеличивается в результате алкоголь индуцированного снижения митохондриального глутатиона, предполагая, что митохондрия основная цель для TNF-alpha. Длительное употребление алкоголя изменяет внутриклеточный баланс между уровнем S-adenosylmethionin и S-adenosylhomocystein, приводя к уменьшению отношения S-adenosylmethionin к S-adenosylhomocystein. Уменьшение этого отношения может способствовать алкоголь индуцированному повреждению печени, так как S-аденозилгомоцистеин усугубляет гепатотоксичность TNF-alpha, тогда как S-аденозилметионин её уменьшает.
Назначение этанола приводит, как к высвобождению митохондриального цитохрома С, так и экспрессии Fas лиганд, что ведет к печеночному апоптозу, через каспаза 3 активируемые пути. В дополнение, согласованные действия TNF-alpha и Fas стимулируемые сигнальные молекулы апоптоза могут повышать чувствительность гепатоцитов к повреждению путем повышения активности натуральных T-киллеров в печени.
Терапия алкогольного гепатита.
Терапия алкогольного гепатита включает, как общие мероприятия для пациентов с декомпенсацией заболеваний печени, так и специфические мероприятия, направленные на вышеописанное повреждение печени (Table 2). Общий подход включает лечение асцита (ограничение соли и диуретики) и лечение энцефалопатии (лактулоза и деконтаминация кишечника). Инфекция должна лечиться соответствующими антибиотиками, подбираемыми по чувствительности индивидуально.
Может понадобиться энтеральное питание, так как пациенты часто аноректичны. Дневная рекомендуемая норма белка - 1,5 г на кг массы тела, даже у пациентов с печеночной энцефалопатией. Тиамин и другие витамины назначаются в соответствии со сводкой диетических рекомендаций. Алкогольный делирий и синдром отмены алкоголя требуют назначения бензодиазепинов, не смотря на возможность усугубления энцефалопатии. Гепаторенальный синдром, требует назначения альбумина и вазоконстрикторов (т. к. терлипресин, мидодрин и октреотид, или норэпинефрин).
Таблица 2. Терапия алкогольного гепатита.
Воздержание от алкоголя.
Немедленное и пожизненное воздержание от алкоголя является необходимым для предотвращения прогрессирования алкогольного гепатита. Мы попросили привлеченных специалистов составить программу психологической и социальной поддержки при воздержании для каждого пациента с алкогольным гепатитом. Пока еще не было исследований эффективности препаратов направленных на подавление тяги к алкоголю при алкогольном гепатите, хотя баклофен, гамма-аминомасленная кислота (GABA) агонист B-рецепторов, по недавним сообщениям, способствует воздержанию от алкоголя на короткий срок в группах активно пьющих пациентов с алкогольным циррозом. К тому же это более безопасно, тогда как безопасность налтрексона, или акампросата у пациентов с алкогольными поражениями печени установлена не была.
Кортикостероиды.
Кортикостероидная терапия обрывает воспалительный процесс, вследствие ингибирования действия транскрипционных факторов, таких как активирующий протеин 1 (AP-1) и NF-kB. При алкогольном гепатите эти эффекты проявляются в виде уменьшения уровня циркулирующих провоспалительных цитокинов интерлейкина 8 и TNF-alpha, растворимых молекул адгезии (soluble intercellular adhesion molecules - SICAM-1) в венозной крови печени, и экспрессией растворимых молекул адгезии (SICAM-1) на мембранах гепатоцитов.
Использование кортикостероидов при лечении алкогольного гепатита было дискутабельным, в силу противоречивых данных индивидуальных исследований и мета-анализа. Недавний мета анализ не говорит в пользу применения кортикостероидов, хотя авторы заключили, что доказательная база – это компромисс между разноречивыми клиническими испытаниями с высоким риском предубежденности. Однако тот же мета анализ показывает, что кортикостероиды в значительной степени снижают смертность в подгруппе из пациентов, дискриминантная функция Маддрея которых, по крайне мере, 32, или с наличием печеночной энцефалопатии, и это исследование было с низким риском предубежденности. Аналогично повторный анализ объединенных индивидуальных данных из трех самых последних исследований, в которых кортикостероиды назначались пациентам на 28 дней, указывает на то, что частота месячной выживаемости у пациентов с тяжелым алкогольным гепатитом (дискриминантная функция Маддрея 32 и более), которые лечились кортикостероидами, была 85%, в сравнении с 65% получавшими плацебо (P=0.001). Наиболее распространенная кортикостероидная терапия при алкогольном гепатите предполагает назначения преднизолона в дозе 40 мг в сутки в течение 28 дней. В конце курса терапии прием преднизолона полностью одномоментно прекращается, либо доза может быть постепенно снижена в течение 3 недель. Показанием для назначения является дискриминантная функция Маддрея 32 и более (или 21 по шкале MELD) в отсутствие сепсиса, гепаторенального синдрома, хронического вирусного гепатита B и желудочно-кишечного кровотечения. Пять пациентов должны пролечиться кортикостероидами для предотвращения одной смерти.
Некоторые данные свидетельствуют, что решение об отмене преднизолона в виду неэффективности может быть принято на основании шкалы Лилла через 7 дней лечения (www.lillemodel.com). Более 0,45 по шкале Лилла свидетельствует о недостаточном ответе на кортикостероиды и предсказывает частоту 6 месячной выживаемости менее 25%.
К сожалению, алкогольный гепатит нечувствительный к кортикостероидам встречается в 40% случаев. Но в таких случаях свою эффективность показали другие препараты, такие как пентоксифиллин (см. ниже).
Кортикостероиды не показаны пациентам с дискриминантной функцией Маддрея менее 32, или менее 21 по шкале MELD, пока не будут доступны данные позволяющие идентифицировать пациентов с высоким риском смертности в короткий период времени.
Пентоксифиллин.
В одном рандомизированном контролируемом исследовании было показано, что пентоксифиллин, ингибитор фосфодиэстеразы с множеством эффектов, включая управление транскрипцией TNF-alpha, уменьшает краткосрочную смертность у пациентов с алкогольным гепатитом. В этом исследовании 101 пациент с дискриминантной функцией Маддрея 32 и более получали наравне с плацебо 400 мг пентоксифиллина 3 раза в сутки на протяжении 28 дней. Никто из пациентов не получал кортикостероиды. 12 из 49 пациентов в пентоксифиллиновой группе (24%) и 24 из 52 пациентов в группе плацебо (46%) погибли в течение первичной госпитализации (P<0.01). Причиной смерти у 6 из 12 пациентов (50%) в пентоксифиллиновой группе и 22 из 24 в (92%) в группе плацебо стал гепаторенальный синдром. Любопытно, что уровни TNF-alpha не имели значительных различий в обеих группах во время исследования, что свидетельствует об эффективности пентоксифиллина, возможно, не зависящей от TNF-alpha. Мы предположили, что, хотя, кортикостероиды влияют на печеночное воспаление, польза от пентоксифиллина может быть в предупреждении гепаторенального синдрома. Не смотря на отсутствие подтверждающих исследований, пентоксифиллин это препарат, заслуживающий внимания для некоторых пациентов.
Анти TNF-alpha терапия.
В качестве терапии алкогольного гепатита исследовались два анти TNF-alpha препарата: инфликсимаб и этанерцепт. Три небольших предварительных исследования инфликсимаба (два не рандомизированных и одно рандомизированное) имели воодушевляющие результаты и привели к проведению более обширных исследований эффективности этого препарата. В результирующих рандомизированных, контролируемых клинических испытаниях сравнивали эффекты в/в инфузий инфликсимаба плюс преднизолон с эффектами плацебо плюс преднизолон у пациентов с тяжелым алкогольным гепатитом (дискриминантная функция Маддрея 32 и более). Впрочем, исследования были прекращены прежде, чем независимые данные при безопасном мониторинге были получены, из-за значительного увеличения тяжелых инфекций и незначительного повышения смертности в когорте с инфликсимабом. Доза инфликсимаба (10 мг на кг веса тела 3 раза в сутки в/в на 1,14 и 28 день) была расценена как чрезмерно высокая, в сравнении с однократной дозой в 5 мг на кг веса тела при других исследованиях.
Этанерцепт показал увеличение краткосрочной выживаемости у пациентов с алкогольным гепатитом в небольшом опытном исследовании, хотя последующее рандомизированное, плацебо-контролируемое испытание, проведенное теми же исследователями, показало худшую 6 месячную выживаемость пациентов в сравнении с группой плацебо. По нашему мнению анти TNF-alpha препараты не должны использоваться для лечения алкогольного гепатита вне клинических испытаний для лечения алкогольного гепатита.
Нутритивная поддержка.
Все пациенты с алкогольным гепатитом имеют алиментарное истощение, и риск гибели сильно коррелирует со степенью истощения. Парентеральное и энтеральное питание улучшает нутритивный статус, но не увеличивает краткосрочной выживаемости. В рандомизированных, контролируемых испытаниях сравнили зондовое питание (2000 ккал в сутки) с преднизолоновой терапией (40 мг преднизолона в сутки) в течение 28 дней у 71 пациента с тяжелым алкогольным гепатитом. Выживаемость в двух группах была сходной в течение 28 дней и в течение года, что предполагает равную эффективность нутритивной поддержки и кортикостероидов у некоторых пациентов.
Другие виды фармакологической поддержки.
Анаболические андрогеновые стероиды, увеличивающие мышечную массу у здоровых субъектов, не улучшают выживаемость при алкогольном гепатите. Исследование лечения антиоксидантами, такими как витамин Е, и силимарин (активный ингредиент расторопши), не показало какого-либо улучшения выживаемости у пациентов, как с алкогольным гепатитом, так и с циррозом, не смотря на то, что алкогольная болезнь печени сопровождается повышенным оксидативным стрессом.
Трансплантация печени.
Алкогольный гепатит до настоящего времени рассматривается как абсолютное противопоказание для трансплантации печени, на тех основаниях, что пациенты с этим расстройством алкоголизировались совсем недавно и такой период воздержания часто дает много шансов на выздоровление. Большинство трансплантационных программ в США сейчас требуют 6 месячного воздержания, прежде чем пациент с алкогольным гепатитом сможет стать годным для трансплантации. К сожалению, многие пациенты погибают во время этого периода, а пациенты, которые поправляются, на максимальном медикаментозном лечении, уже хорошо изучены прежде, чем пройдут 6 месяцев. Вельд, в частности, считает, что пациенты с печеночной недостаточностью вследствие алкогольной болезни печени, которые не поправились, в течение 3 месяцев воздержания, вряд ли выживут. Таким образом, центры трансплантации стоят перед дилеммой - когда брать пациентов с алкоголизмом, и алкогольным гепатитом, чьё состояние ухудшается, не смотря на строгое воздержание, нутритивную поддержку, кортикостероиды и другие элементы медикаментозного лечения. Возврат к употреблению алкоголя после трансплантации так же вызывает обеспокоенность.
Заключение.
Диагностика алкогольного гепатита основывается на данных анамнеза (массивная длительная алкоголизация), наличии желтухи и отсутствии других причин для гепатита. Биопсия печени – это важное диагностическое средство, но бесполезное, как для определения прогноза, так и для установления сроков алкоголизации и воздержания. Воздержание от алкоголя – краеугольный камень лечения. Истощенные пациенты требуют калорийной и белковой поддержки. Пациентам с тяжелым алкогольным гепатитом, у которых нет сепсиса, следует назначать преднизолон в дозе 40 мг в сутки на 28 дней. Через 7 дней лечения кортикостероидами, у пациентов, набравших по шкале Лилл более 0.45, может быть заболевание не чувствительное к кортикостероидам, или к раннему включению пентоксифиллина. Когда клиническая ситуация такова, что врачи вынуждены назначать кортикостероиды, пентоксифиллин может оказаться полезным для предупреждения гепаторенального синдрома, который может привести к смерти. Эффективность совместного лечения пентоксифиллином и кортикостероидами не изучена и требует рандомизированных, контролируемых исследований. Пациенты с менее тяжелым алкогольным гепатитом, степень краткосрочной выживаемости которых достигает 90%, не должны лечиться кортикостероидами, из-за риска таких осложнений, как системные инфекции. В завершении есть необходимость в хорошо проведенных исследованиях трансплантации печени у аккуратно подобранных пациентов с тяжелым алкогольным гепатитом нечувствительным к медикаментозному лечению.
Dr. Lucey reports receiving consulting fees from Astellas Pharma and grant support from Bristol-Myers Squibb, Human Genome Sciences, Integrated Therapeutics, Salix, Vertex, Roche, Schering-Plough, and Idenix; Dr. Mathurin, consulting fees from Vertex, Sanofi-Aventis, Gilead, Roche, Schering-Plough, Bristol-Myers Squibb, and Bayer HealthCare and lecture fees from Roche, Gilead, Schering-Plough, Bristol-Myers Squibb, and Bayer HealthCare; and Dr. Morgan, consulting fees from Gilead, Roche, and Vertex, lecture fees from Roche and Schering Plough, and grant support from Roche, Schering-Plough, and Vertex. No other potential conflict of interest relevant to this article was reported.
Оригинал статьи
| Количество просмотров: 29453 |
Комментарии к статье
Стас | 2011-02-15, 05:54
Отлично!!! Не врачи, не лезьте! Есть интернет, а есть специалисты! Они мало пересекаются...